Jubel bei den Biofrontera-Aktionären: Der Spezialist für die Behandlung von sonneninduziertem Hautkrebs hat die schriftliche Stellungnahme der amerikanischen Arzneimittelbehörde FDA zu den Bedingungen der Zulassung von Ameluz für das Basalzellkarzinom in den USA erhalten. Entsprechend dem vereinbarten Entwicklungsplan kann die Zulassungserweiterung auf superfizielle Basalzellkarzinome auf Basis einer einzigen ergänzenden, in den USA durchgeführten Phase-3-Studie beantragt werden, bei der Ameluz mit einem Placebo verglichen wird. Die FDA erwartet von Biofrontera eine kombinierte Auswertung der klinischen und histologischen Heilungsraten. Die klinische Untersuchung von Patienten mit unterschiedlichem ethnischen Hintergrund oder Kindern wird nicht gefordert. Aufgrund der hohen Wirksamkeit von Ameluz (ca. 95 Prozent Heilungsrate bei superfiziellen Basalzellkarzinomen in der europäischen Studie) und der niedrigen Rezidivraten (5,4 Prozent nach 12 Monaten), kann die geforderte Placebo-kontrollierte Studie mit relativ wenigen Patienten durchgeführt werden, wodurch der Zeitaufwand und die Kosten minimiert werden. Hinsichtlich der Sicherheitsinformationen und Langzeitdaten hat die FDA die vorhandene europäische Studie zum Review akzeptiert.
„Die US-Dermatologen würden eine Zulassungserweiterung von Ameluz auf superfizielle Basalzellkarzinome sehr begrüßen, denn es fehlt uns an guten Alternativen zur Chirurgie – vor allem was größere Tumoren angeht, die chirurgisch schwer zu entfernen sind“, sagte Dr. David M. Pariser, leitender Arzt der Pariser Dermatology Specialists in Norfolk, Virginia, und seit 40 Jahren praktizierender Dermatologe, der bei dem Treffen mit der FDA als medizinischer Berater im Auftrag von Biofrontera tätig war.
„Die FDA hat sich mit der Zustimmung zu einer einzigen Placebo-kontrollierten pivotalen Studie in den USA als Zulassungsvoraussetzung für Ameluz bei superfiziellen BCCs sehr flexibel gezeigt. Dies illustriert das Bemühen der Behörde, Unternehmen dabei zu unterstützen, neue Medikamente in einem angemessenen Zeit- und Kostenrahmen auf den Markt bringen zu können“, so Prof. Dr. Hermann Lübbert, Biofronteras Vorstandsvorsitzender.
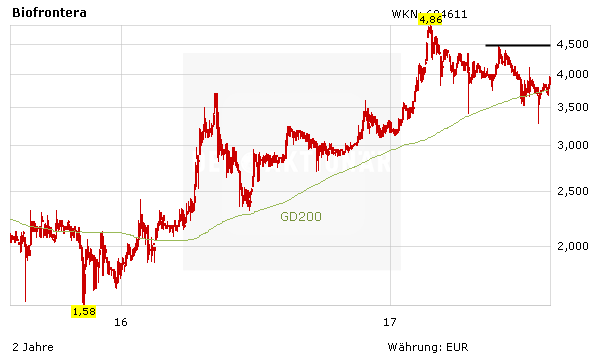
Aktie mit deutlichem Kurssprung
Die Aktie von Biofrontera reagierte auf die heute Meldung mit einem deutlichen Kursplus von mehr als sieben Prozent auf 3,94 Euro. Damit konnte die 200-Tage-Linie klar übersprungen werden. Mit den jüngsten starken News im Rücken dürfte die Aktie ihre Aufholbewegung fortsetzen können. Die nächste größere Hürde wartet aus charttechnischer Sicht im Bereich von 4,50 Euro. DER AKTIONÄR spekuliert im Real-Depot auf dieses Szenario.
Hinweis nach §34 WPHG zur Begründung möglicher Interessenkonflikte: Aktien oder Derivate, die in diesem Artikel besprochen / genannt werden, befinden sich im "Real-Depot" von DER AKTIONÄR.

 DER AKTIONÄR – Unsere App
DER AKTIONÄR – Unsere App


